PROPRIEDADES FÍSICAS
DOS ALCINOS
Os alcinos de
cadeia normal, de C2 a C4 são gases; de C5 a C14
são líquidos e de C15 em diante são sólidos em condições ambientes.
Os pontos de fusão e de ebulição dos alcinos aumentam com o aumento da massa
molecular (aumento da cadeia carbónica).
Os alcinos são
incolores, inodoros, insolúveis em água e solúveis em solventes orgânicos. Excepcionalmente,
o primeiro membro da série homóloga dos alcinos, o Etino (acetileno), tem
cheiro agradável e é parcialmente solúvel em água.
PROPRIEDADES QUÍMICAS
DOS ALCINOS
Os alcinos tal
como os alcenos sofrem tipicamente reacções
de adição. No entanto, devido à presença de uma tripla ligação (que é
instável), os alcinos apresentam uma actividade química um pouco mais
pronunciada que a dos alcanos e alcenos, portanto, os alcinos são mais reactivos que os alcanos e alcenos.
Nos alcinos destacam-se as reacções
de adição, oxidação-redução e polimerização.
1. REACÇÃO DE ADIÇÃO
⦁ Hidrogenação
(adição de hidrogénio)
Na
hidrogenação parcial de um alcino forma-se um alceno e na hidrogenação total
forma-se um alcano.
Hidrogenação parcial: é adicionado um mol de hidrogénio (H2) causando a quebra de uma ligação química e formando-se um alceno.
Hidrogenação total: são adicionados dois moles de hidrogénio (2H2) quebrando-se duas ligações químicas formando-se um alcano.
⦁ Halogenação (adição de halogéneos)
Esta reacção ocorre em duas etapas. Primeiro é adicionada uma molécula de halogéneo formando-se um dialeto insaturado e a este é adicionada mais uma molécula de halogéneo formando-se um tetraleto.
⦁ Adição de hidrácido
Os alcinos adicionam haletos de hidrogénio (HX) para formar dialetos segundo a Regra de Markovnikov.
Os alcinos adicionam também o ácido cianídrico (HCN) formando cianetos
(nitrilos) insaturados.
⦁ Hidratação (adição de água)
Os alcinos
adicionam a água quando tratados com ácido sulfúrico diluído na presença do
Sulfato de Mercúrio II (HgSO4) como catalisador para formar aldeído
ou cetonas.
Partindo do Etino, por exemplo, inicialmente forma-se um composto instável chamado enol. Este enol por ser instável sofre um rearranjo estrutural, num processo denominado de Tautomeria. Assim, estabelece-se um equilíbrio dinâmico aldo-enólico de modo que coexistem tanto o enol assim como o aldeído (com predominância do aldeído).
Quando um alcino diferente do Etino é utilizado formam-se cetonas e não aldeídos pelo facto de se obedecer a Regra de Markovnikov.
Neste caso
estabelece-se então um equilíbrio ceto-enólico.
2. REACÇÕES DE OXIDAÇÃO-REDUÇÃO
⦁ Reacções de
combustão completa: produz-se água e dióxido de carbono.
2 C2H2
+ 5 O2 → 4 CO2
+ 2 H2O
⦁ Reacções de
combustão incompleta: produz-se água e monóxido de carbono ou carbono
(fuligem).
2 C2H2
+ 3 O2 → 4 CO + 2 H2O
2 C2H2
+ O2 → 4 C + 2 H2O
⦁ Oxidação branda: os alcinos sofrem oxidação branda quando tratados com uma solução aquosa neutra ou levemente alcalina de permanganato de potássio (KMnO4) para produzir dicetonas.
⦁ Oxidação
enérgica: os alcinos sofrem oxidação enérgica quando tratados com uma
solução ácida concentrada de KMnO4, sob aquecimento.
Se o carbono
da tripla ligação não possui hidrogénio, ele se converte em carboxila e se
possui hidrogénio, ele converte-se em CO2.
3. POLIMERIZAÇÃO
⦁ Trimerização
do acetileno para formar o benzeno.
Por: Miguel Pascoal
Licenciado em Ensino de Química
full-width






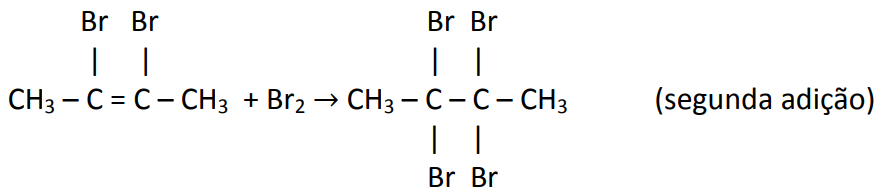











0 Comentários