RESOLUÇÃO DO EXAME
DE QUÍMICA DA 10a CLASSE – 1a CHAMADA – 2022
1. Dado o símbolo 32Ge73
a) Faça a distribuição electrónica do átomo.
b) Localize o átomo na Tabela Periódica, indicando o grupo e o período.
RESOLUÇÃO
a) A distribuição electrónica do átomo deste
elemento é a seguinte:
K – 2e-; L – 8e-;
M – 18e-; N – 4e-
b) O grupo é
indicado pelo número de electrões da camada de valência (última camada) e o período é indicado pelo número de
níveis de energia (camadas) preenchidos pelos electrões desse átomo.
Na distribuição
electrónica que acabamos de fazer, a última camada (camada de valência) é N que
tem quatro (4) electrões, portanto, este elemento localiza-se no quarto grupo
principal (Grupo IV A) da Tabela Periódica.
Por outro lado, os níveis
de energia que os electrões do átomo deste elemento preenchem são K, L, M e N,
portanto, são 4 níveis de energia, o que significa que este elemento
localiza-se no quarto período (4o período) da Tabela Periódica.
Resposta: Grupo: IV A e 4o período.
2. Os compostos abaixo são de carbono e inorgânicos.
I. CO II. H2CO3
a) Nomeie os compostos abaixo.
b) Escreva a equação química acertada da reacção entre o composto II e o hidróxido de cálcio.
RESOLUÇÃO
a) I. O CO é um óxido não metálico, assim, a regra para a sua nomenclatura
pode ser escrita como:
prefixo + óxido + de + nome do elemento ligado ao
oxigénio
Ora, temos um átomo de Oxigénio, pelo que o prefixo é mono. Portanto, pimeiro vamos escrever o prefixo mono,
de seguinda a palavra óxido, depois
a preposição “de” e por fim o nome
do elemento ligado ao Oxigénio que no
caso é o Carbono:
Mono + óxido + de + carbono = monóxido
de carbono.
II. O H2CO3 é um ácido oxigenado,
assim, a regra da nomenclatura para este ácido pode ser escrita como:
Ácido + nome do elemento central + ico
Como se vê, primeiro
escreveremos a palavra ácido, de seguida o nome do elemento central que no caso
é o carbono e terminaremos com a terminação ico, de modo que o nome deste ácido
é:
Ácido + carbono + ico = Ácido carbónico
Resposta: I. Monóxido de carbono e II. Ácido carbónico.
b) O ácido carbónico é um
ácido e o hidróxido de cálcio é uma base. A reacção entre um ácido e uma base
designa-se reacção de neutralização.
Os produtos de uma reacção de neutralização são um sal e água.
Ácido + base → Sal + água
Assim, a equação da
reacção acertada é:
H2CO3(aq) + Ca(OH)2(aq) → CaCO3(aq) + 2 H2O(l)
3. Dado o composto CH3 – CH = CH – CH2
– NO2
Passe para a sua folha de
respostas a opção que classifica correctamente a cadeia do composto
A Alifática, normal, insaturada e homogénea.
B Aberta, ramificada, saturada e homogénea.
C Acíclica, ramificada, insaturada e homogénea.
D Alifática, normal, insaturada e heterogénea.
RESOLUÇÃO
A cadeia apresentada (CH3
– CH = CH – CH2 – NO2) apresenta átomos de carbono em
que as extremidades não se ligam entre si formando um ciclo, pelo que trata-se
de uma cadeia aberta, alifática ou acíclica. A mesma cadeia não apresenta ramificações, logo é uma cadeia normal. Esta cadeia apresenta
uma dupla ligação entre os átmos de
carbono, por isso é uma cadeia
insaturada e é homogénea porque
entre os átomos de carbono não existe um heteroátomo
(um átomo diferente de carbono).
Resposta: Alternativa: A
4. Os compostos abaixo pertencem a diferentes funções
orgânicas.
I. CH3 – CH = CH – CH3
II. CH3 – CH2 – CO – CH3
III. CH3 – CH2 – CH2
– CHO
Indique a função química
de cada um dos compostos.
RESOLUÇÃO
I. CH3 – CH =
CH – CH3 ⇒ Apresenta somente átomos
de carbono e Hidrogénio, logo é um Hidrocarboneto (alceno).
II. CH3 – CH2
– CO – CH3 ⇒ apresenta o grupo
carbonilo (– CO –) logo é uma Cetona.
III. CH3 – CH2
– CH2 - CHO ⇒ apresenta o grupo
aldoxila (– CHO) logo é um Aldeído.
5. Observe as substâncias que se seguem.
a) Represente a fórmula
racional da substância I.
b) Escreva o nome da
substância II segundo a IUPAC
RESOLUÇÃO
a) O nome do composto nos indica que a cadeia principal
tem 5 átomos de carbono (prefixo “penta”) e trata-se de um alceno, visto que
temos o infixo “en”. O número dois (2) no fim do nome nos indica que a dupla
ligação localiza-se entre os carbono 2 e 3. Por fim, nos carbonos 2 e 3 temos
radiciais metil respectivamente.
b) Etilbenzeno
6. Leia atentamente as frases abaixo.
I. O benzeno é o hidrocarboneto aromático mais simples.
II. O benzeno é um gás de
odor agradável e imiscível com a água
III. O benzeno é um
solvente importante na indústria química
IV. O benzeno apresenta
cinco átomos de carbono e cadeia fechada.
Passe para a sua folha de
respostas às frases verdadeiras.
RESOLUÇÃO
O benzeno é o
hidrocarboneto aromático mais simples, com seis átomos de Carbono e 6 átomos de
Hidrogénio. Algumas propriedades físicas do benzeno e suas aplicações, que são:
É um líquido incolor, com um odor doce a essências, mas bastante tóxico. É
solúvel em éter, nafta, e acetona, no álcool e outros
solventes orgânicos. Por ser uma substância apolar é imiscível com a água. O
benzeno é menos denso do que a água, com uma densidade de 0,89 g/cm3.
O Ponto de ebulição do benzeno é de 80,1o
C e ponto de fusão é igual a 5,5oC.
O benzeno é
principalmente usado como solvente orgânico assim como na produção de várias
substâncias químicas tais como, pesticidas, explosivos, corantes, tintas, etc.
Resposta: I. O benzeno é o
hidrocarboneto aromático mais simples; e III. O benzeno é um solvente
importante na indústria química.
7. Observe os álcoois abaixo.
a) Nomeie o composto I
segundo a nomenclatura IUPAC
b) Nomeie o composto II
segundo a nomenclatura usual
c) Classifique o álcool I
quanto à posição do grupo hidroxila e quanto ao número de grupos hidroxila.
RESOLUÇÃO
a) 2,2 – Dimetil-pentanol – 3
b) Álcool isopropílico.
c) Quanto à posição do
grupo hidroxila: álcool secundário.
Quanto ao número de
grupos hidroxila: monoálcool ou monol.
8. As fórmulas abaixo são de compostos orgânicos
oxigenados.
I CH3 – COH;
II. C2H2(OH)2;
III. CH3 – CH2 – OH;
a) Qual delas é do álcool
etílico?
b) Mencione três (3)
propriedades físicas do álcool etílico.
RESOLUÇÃO
a) A fórmula do álcool
etílico ou etanol é III. CH3 – CH2 – OH.
b) As propriedades
físicas do álcool etílico são: é um líquido incolor, inflamável e é solúvel em
água.
9. Dado o composto
a) Escreva um (1) isómero
de cadeia do composto.
b) Nomeie o isómero que
escreveu na alínea 9.a).
RESOLUÇÃO
a) Isómeros são compostos
que têm a mesma fórmula molecular mas estruturas diferentes. Neste caso, o
isómero pode ser: CH3 – CH2 – CH2 – CH2
– CH2 – OH.
b) O nome é: pentanol –
1.
10. Complete e acerte as equações químicas abaixo.
RESOLUÇÃO
a) Esta reacção corresponde a Síntese de Dumas, um dos métodos de obtenção dos alcanos.
b) Esta é uma reacção de adição que ocorre nos alcenos, aplica-se aqui a Regra de Markovnikov.
c) Trata-se de uma reacção de oxidação. Na presença de agentes oxidantes, como tais como Permanganato de Potássio (KMnO4) ou Dicromato de Potássio (K2Cr2O7) os álcoois primário se oxidam dando origem a um aldeído (oxidação parcial) e este se oxida formando um ácido carboxílico (oxidação total).
11. Qual é o conteúdo da regra que usou ao completar a
equaçã0 10.b)?
RESOLUÇÃO
O conteúdo da regra é: em reações de adição, o radical do ácido ou outro composto, liga-se ao carbono menos hidrogenado da dupla ligação e o hidrogénio ao carbono mais hidrogenado.
12. Escreve e acerte a equação química da reacção entre o
propanol – 1 e o sódio.
RESOLUÇÃO
Os álcoois têm carácter ácido devido à
polaridade da ligação O – H, por isso reagem com metais alcalinos, libertando o gás
hidrogénio.
2 CH3 – CH2 – CH2 – OH + 2 Na → 2 CH3 – CH2 – CH2 – ONa + H2
Por: Miguel Pascoal
full-width
Exame
de Química 2019 Segunda época; Guia de correcção de exames 2021
Exames
de quimica 10o classe pdf 2021; Exames de quimica 10o
classe pdf 2019
Exames
de quimica 10o classe 2021; Exames de quimica 10o classe
pdf 2020 guia
Exames
de quimica 10o classe pdf 2018; exames da 10o classe 2020
exames resolvido
Exame
de química 10a Classe guia de correcção.
Exame
de Química 2022 1a Chamada, Segunda época; Guia de correcção de
exames 2021







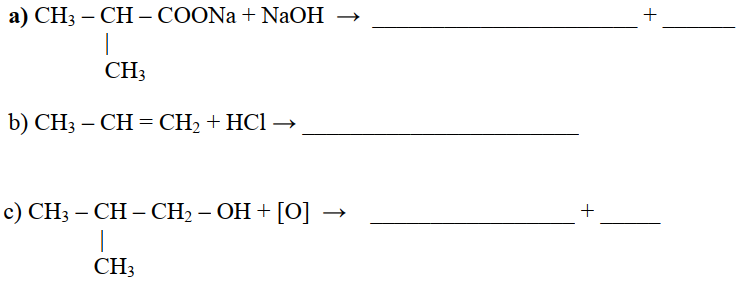








0 Comentários