RESOLUÇÃO DO EXAME
DE QUÍMICA DA 10a CLASSE – 1a CHAMADA – 2021
1. O átomo de um determinado elemento possui 15 electrões
e 16 neutrões.
a) Qual é o seu número atómico?
b) Calcule o número de massa do átomo.
RESOLUÇÃO
a) Num átomo neutro, o número de electrões (e-) é igual ao
número de protões (p+). Dado que este átomo é neutro, significa que e- = p+ mas e- = 15 electrões, logo:
e- = p+ = 15
O número atómico (Z) é a quantidade de protões (p+) que
existe no núcleo de um átomo (Z = p+).
Ora, se o número de protões (p+)
é igual a 15 significa que o número atómico também é igual a 15 visto que Z = p+:
Z = p+ = 15.
Resposta: o número atómico é igual a 15.
b) O número de massa (A) é calculado através da seguinte
fórmula:
A = Z + N
O Z é o número atómico
que é igual a 15 e o N é o número de neutrões que é igual a 16, assim, o
número de massa é:
A = Z + N
A = 15 + 16
A = 31
2. O número atómico do cálcio é 20. Os electrões do cálcio estão distribuídos em:
A 2 camadas
B 3 camadas
C 4 camadas
D 5 camadas
RESOLUÇÃO
Para saber em quantas camadas estão distribuídos os electrões de cálcio
temos que efectuar a distribuição electrónica do átomo deste elemento.
20Ca: K – 2e-; L – 8e-; M – 8e-; N – 2e-
Como se vê, temos as seguintes camadas, K, L, M e N, portanto, são 4 camadas.
Resposta: alternativa: C
3. Dados os compostos.
I: CaO II:
NH3 III: HCl IV:
MgI2
a) Quais são os compostos formados por ligação iónica?
b) Que tipo de rede cristalina possui o composto III?
RESOLUÇÃO
a) Para responder correctamente é necessário saber o que é uma ligação iónica. Uma ligação iónica é a força electrostática que mantém os iões unidos numa
substância iónica. A ligação iónica se estabelece entre átomos de elementos
metálicos (os metais) e átomos de
elementos não metálicos (os não metais
ou ametais).
Análise dos
itens
I. CaO ⇒ O Cálcio (Ca) é um metal e o Oxigénio (O) é um não ametal, então entre
estes átomos se estabele uma ligação iónica.
II. NH3 ⇒ O Nitrogénio (N) é um não metal e o Hidrogénio (H) também pode ser classificado como não metal. Entre átomos de elementos não metálicos estabelece-se uma ligação covalente e não a ligação iónica.
III. HCl ⇒ O Cloro (Cl) é um não metal e o Hidrogénio (H) também pode ser classificado como não metal. Entre átomos de elementos não metálicos estabelece-se uma ligação covalente e não a ligação iónica.
IV. MgI2 ⇒ O Magnésio (Mg) é um metal e o
Iodo (I) é um não ametal, então entre estes átomos se estabele uma ligação iónica.
Resposta: I e IV.
b) Nas moléculas de HCl, os átomos estão ligados entre si por meio de ligações
covalentes. Portanto, o HCl é uma substância covalente ou molecular, ou seja,
possui rede covalente ou rede molecular.
Resposta: Rede covalente ou rede
molecular.
4. As frases abaixo são sobre as ligações químicas.
I. Entre os átomos de alumínio existe ligação covalente;
II. Entre os átomos de
bromo existe a ligação iónica;
III. Entre os átomos de
bário e oxigénio existe a ligação iónica;
IV. Entre os átomos de
alumínio existe a ligação metálica.
RESOLUÇÃO
Vamos analisar cada um
dos itens dados:
I . INCORRECTO
O Alumínio (Al) é um
metal. Os átomos de elementos metálicos encontram-se ligados entre si por meio
de ligações metálicas.
II. INCORRECTO
O Bromo (Br) é um
elemento não metálico. Os átomos de elementos não metálicos encontram-se
ligados entre si por meio de ligações
covalentes.
III. CORRECTO
O Bário (Ba) é um metal e o Oxigénio (O) é um não ametal,
então entre estes átomos se estabele uma ligação
iónica.
IV. CORRECTO
O Alumínio (Al) é um
metal. Os átomos de elementos metálicos encontram-se ligados entre si por meio
de ligações metálicas.
Resposta: III e IV.
5. O efeito de estufa não é sinónimo de problema. Ele é
necessário e bom.
Qual é a importância do efeito de estufa?
RESOLUÇÃO
O efeito de estufa é importante porque possibilita a manutenção da
temperatura da terra numa média de 15oC, ideal para o equilíbrio de
grande parte das formas de vida em nosso planeta. Sem o efeito estufa natural,
o planeta Terra poderia ficar muito frio, inviabilizando o desenvolvimento de
grande parte das espécies animais e vegetais. Isso ocorreria, pois, a radiação
solar reflectida pela Terra se perderia totalmente.
6. O ácido carbónico apresenta as mesmas propriedades
químicas dos outros ácidos inorgânicos. Escreva a equação química acertada
desse ácido com o hidróxido de sódio.
RESOLUÇÃO
Numa equação química
temos os reagentes que são as substâncias que ficam antes da seta e os produtos
que ficam depois da seta. Neste caso os reagentes são o ácido carbónico (H2CO3)
o hidróxido de sódio (NaOH).
O ácido carbónico é um
ácido e o hidróxido de sódio é uma base. A reacção entre um ácido e uma base
designa-se reacção de neutralização.
Os produtos de uma reacção de neutralização são um sal e água.
Ácido + base → Sal + água
Assim, a equação da
reacção acertada é:
H2CO3(aq) + 2 NaOH(aq) → Na2CO3(aq)
+ 2 H2O(l)
7. Dada a seguinte cadeia carbónica
Classifique os átomos de
carbono.
RESOLUÇÃO
Classificação dos átomos de carbono numa cadeia carbónica
• Carbono
primário: é aquele que está ligado a no
máximo um outro átomo de carbono;
• Carbono
secundário: é aquele que está ligado a no
máximo dois (2) outros átomos de carbono;
• Carbono
terciário: é aquele que está ligado a no
máximo três (3) outros átomos de carbono;
• Carbono quaternário é aquele que está ligado a no máximo quatro (4) outros átomos de carbono.
Analisando a cadeia carbónica temos:
Carbono primário: 1, 5, 6, 7 e 8
Carbono secundário: 4
Carbono
terciário: 2
Carbono quaternário: 3
8. Observe os compostos abaixo.
I CH ≡ CH; II. CH3 – CO – CH3; III.
CH3 –
CH3; IV. CH3 – CHO
Identifique a subfunção
ou função a que pertence cada composto.
RESOLUÇÃO
I. CH ≡ CH ⇒ é um
hidrocarboneto com ligação tripla, logo é um Alcino.
II. CH3 – CO –
CH3 ⇒ apresenta o grupo carbonilo (– CO –) logo é uma Cetona.
III. CH3 – CH3
⇒ é um
hidrocarboneto com ligações simples, logo é um Alcano;
IV. CH3 – CHO ⇒ apresenta o
grupo aldoxila (– CHO) logo é um Aldeído.
9. Observe os seguintes compostos.
a) Escreve os nomes oficiais dos compostos I e II.
b) Nomeie o composto III segundo a nomenclatura usual.
RESOLUÇÃO
a) I. Propil-Benzeno
II. 2 –
Metil-Propeno
b) III. Dimetilmetano
10. Observe os compostos abaixo.
Represente os isómeros
geométricos e escreva os respectivos nomes para o composto que obedece ao
Princípio de isomeria geométrica.
RESOLUÇÃO
A isomeria
cis/trans ocorre em compostos que apresentam ligação dupla (alcenos) ou em
cicloalcanos. Uma maneira de identificar se um alceno possui isomeria
geométrica é comparar os ligantes em cada átomo de carbono da dupla ligação. Se
eles são iguais em um dos átomos de carbono, não ocorre isomeria
geométrica. Caso os ligantes forem
diferentes em cada átomo de carbono, o composto apresentará isomeria
geométrica.
Quando os ligantes iguais estão em lados opostos ao plano imaginário que contém a dupla ligação, o isómero é chamado de trans. Se os ligantes iguais estão no mesmo lado, o isómero é cis. A isomeria geométrica nos cicloalcanos ocorre quando pelo menos dois átomos de carbono do anel possuem dois ligantes diferentes entre si.
11. Complete a acerte as equações que se seguem.
RESOLUÇÃO
Por: Miguel Pascoal
full-width
Exame
de Química 2019 Segunda época; Guia de correcção de exames 2021
Exames
de quimica 10o classe pdf 2021; Exames de quimica 10o
classe pdf 2019
Exames
de quimica 10o classe 2021; Exames de quimica 10o classe
pdf 2020 guia
Exames
de quimica 10o classe pdf 2018; exames da 10o classe 2020
exames resolvido
Exame
de química 10a Classe guia de correcção.




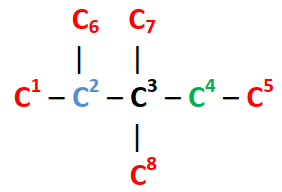










0 Comentários